Bases de Registros de Protocolos de Ensaios Clínicos
Publicado por 3 de Novembro de 2022 em Estudantes para Melhores Evidências

Introdução
Bases de registros de protocolos de ensaios clínicos são arquivos eletrônicos, de livre acesso, onde autores de ensaios clínicos devem obrigatoriamente registrar as informações pertinentes ao estudo, antes de seu início, atualizá-las durante sua realização e disponibilizar seus resultados, independentemente dos seus achados [1,2].
Objetivos do registro
Os objetivos das bases de registros de protocolos de ensaios clínicos envolvem aspectos éticos e científicos como apresentado no Quadro 1 [1].
Quadro 1. Objetivos dos registros de protocolos de ensaios clínicos – adaptado de [1].
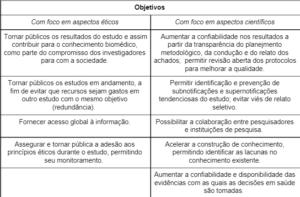
Vale destacar que quando é realizada a análise crítica de um artigo relatando um ensaio clínico, dois dos itens que devem ser considerados são: (i) a existência do número de registro, que deve estar explícito no artigo publicado e (ii) a confirmação de que este registro foi prospectivo, ou seja, realizado antes da inclusão do primeiro paciente.
Obrigatoriedade do registro
O registro obrigatório tem três componentes:
- obtenção de um número internacional de identificação do estudo;
- registro do protocolo original junto a adendos subsequentes;
- relato dos resultados – com a inserção dos dados na própria plataforma, link para outro website ou ainda o link para o artigo publicado com os resultados finais [1].
Atualmente, o International Committee of Medical Editors (ICMJE, em português Comitê Internacional de Editores de Revistas Médicas) recomenda que as revista científicas signatárias exijam o número de registro do protocolo do ensaio clínico no momento da submissão do manuscrito que relata o estudo [2,4].
Bases para registro
As bases de registro mais conhecidas são:
- International Clinical Trials Register Platform (ICTRP, mantida pela Organização Mundial da Saúde – OMS) e que integra os registros de diversas bases de dados regionais ou nacionais. Disponível em https://www.who.int/clinical-trials-registry-platform.
- ClinicalTrials.gov (mantida pelo National Institute of Health – NIH, EUA). Disponível em https://clinicaltrials.gov/.
Uma lista completa de bases de dados para registros de protocolos de ensaios clínicos pode ser encontrada no Portal da rede Biblioteca Virtual em Saúde (BVS) em: https://red.bvsalud.org/lilacs/pt/lista-bases-para-registro-de-ensaios-clinicos/ [3].
No Brasil, há o Registro Brasileiro de Ensaios Clínicos (ReBEC), administrado pela Fundação Oswaldo Cruz (Fiocruz), em parceria com a Organização Pan-Americana de Saúde (Opas) [4] e disponível em https://ensaiosclinicos.gov.br/.
Autores: Lorena Dal Collina Sangiuliano, Luiza Martins Berbel, Priscila Giusti Lázaro, Tatiane Lissa Yamada, Thais Mie Hoshino e Victor Alexandre dos Santos Valsecchi. Alunos de graduação da Escola Paulista de Medicina (EPM), Universidade Federal de São Paulo (Unifesp).
Supervisoras: Rachel Riera. Professora adjunta, Disciplina de Medicina Baseada em Evidências, Escola Paulista de Medicina (EPM), Universidade Federal de São Paulo (Unifesp). Carolina de Oliveira Cruz Latorraca, Associação Paulista para o Desenvolvimento da Medicina (SPDM).
Citar como: Sangiuliano LDC, Berbel LM, Lázaro PG, Yamada TL, Hoshino TM, Valsecchi VAS, COC Latorraca, Riera R. Bases de registros de ensaios clínicos Estudantes para Melhores Evidências (EME) Cochrane. Disponível em: [colar link]. Acessado em [dia, mês e ano].
Referências
- Krleza-Jerić K, Chan AW, Dickersin K, Sim I, Grimshaw J, Gluud C. Principles for international registration of protocol information and results from human trials of health related interventions: Ottawa statement (part 1). BMJ. 2005;330(7497):956-8. doi: 10.1136/bmj.330.7497.956. Erratum in: BMJ. 2005 May 28;330(7502):1258. PMID: 15845980; PMCID: PMC556346.
- Peccin MS. Registro de ensaios clínicos: quando e por que fazer?. Brazilian Journal of Physical Therapy, v. 11, p. v-vi, 2007.Disponível em: https://www.scielo.br/j/rbfis/a/tM5HqqSd3dHzqyXJHBpmkPs/?lang=pt. Acessado em 27 de setembro de 2022.
- BVS Argentina.Lista de Bases para Registros de Ensaios Clínicos. Disponível em: https://red.bvsalud.org/lilacs/pt/lista-bases-para-registro-de-ensaios-clinicos/. Acessado em 27 de setembro de 2022.
- Freitas, Carolina Gomes, et al. “Practical and conceptual issues of clinical trial registration for Brazilian researchers.” Sao Paulo Medical Journal.2915;134:28-33.



